PCV2 em Portugal: diversidade e evolução genotípica, vigilância molecular e apoio à decisão vacinal

O circovírus suíno tipo 2 (PCV2) é um agente patogénico de elevado impacto na suinicultura e, apesar de ser um vírus de ADN, apresenta uma taxa evolutiva elevada, o que favorece o surgimento de variantes e a sua organização em múltiplos genótipos ao longo do tempo. Esta diversidade sustenta a vigilância molecular, a comparação epidemiológica entre regiões e períodos, a discussão sobre virulência e as implicações para a vacinação (Karuppannan & Opriessnig, 2017; Franzo & Segalés, 2020).
Um desafio recorrente é a padronização da genotipagem. Com a expansão da sequenciação e a variabilidade intrínseca do vírus, foram propostas nomenclaturas nem sempre compatíveis, dificultando comparações entre estudos. Para mitigar este problema, foi proposta uma definição de genótipos ancorada na filogenia, com critérios explícitos baseados no gene ORF2, permitindo a delimitação de oito genótipos (PCV2a–PCV2h). Esta abordagem procura estabelecer uma linguagem comum e, simultaneamente, sublinha o potencial enviesamento associado à amostragem (desequilíbrios geográficos, temporais e do hospedeiro), que pode induzir associações aparentes entre genótipos e atributos biológicos/epidemiológicos (Franzo & Segalés, 2018).
Em termos de dinâmica populacional, a literatura descreve ondas de dominância e “genotype shifts”, frequentemente sintetizados como PCV2a → PCV2b → PCV2d. Uma revisão focada em vacinação e epidemiologia molecular refere que as vacinas comerciais foram introduzidas em larga escala por volta de 2006 em populações onde PCV2b predominava e que, a partir de 2012, PCV2d substituiu amplamente PCV2b. Este segundo grande “genotype shift” intensificou a discussão sobre possível alteração de virulência e, sobretudo, sobre o desempenho de vacinas derivadas de PCV2a perante vírus do genótipo PCV2d (Karuppannan & Opriessnig, 2017). Importa ainda salientar que podem ser detetadas, no mesmo animal, diferentes estirpes de PCV2 do mesmo genótipo ou de genótipos distintos, reforçando a complexidade da infeção em contexto de campo (Franzo & Segalés, 2018).
Uma análise filodinâmica recente, beneficiando de maior disponibilidade de sequências ORF2, confirma as três grandes ondas (PCV2a, PCV2b e PCV2d), mas evidencia também que PCV2a e PCV2b podem voltar a flutuar em prevalência após declínios iniciais, sugerindo mecanismos como seleção negativa dependente da frequência, imunidade local e introduções periódicas de linhagens entre regiões. Os autores concluem que, embora PCV2d seja atualmente o genótipo mais prevalente, genótipos minoritários continuam a circular e as estratégias de controlo devem visar a população total de PCV2, promovendo imunidade mais ampla e cruzada (Franzo et al., 2024).
Neste enquadramento, tem sido discutido um potencial aumento do desfasamento genético entre estirpes vacinais e estirpes circulantes. Na seleção de vacinas, pode ser relevante considerar formulações que maximizem a correspondência de epítopos de células T com as estirpes em circulação. Para quantificar a proximidade entre vacinas contra PCV2 e estirpes de campo, foram previstos e comparados conteúdos de epítopos de células T e calculadas pontuações de Epitope Content Comparison (EpiCC), recorrendo a ferramentas validadas (Bandrick et al., 2020).
O CircoMatch™ aplica a ferramenta EpiCC e o algoritmo PigMatrix (EpiVax), através de uma plataforma web, para realizar uma comparação entre vacinas contra PCV2 e estirpes de campo em circulação, disponibilizando uma estimativa preditiva de “cobertura” ao nível de epítopos de células T. Este tipo de abordagem pode apoiar, de forma complementar à caracterização molecular, a tomada de decisão vacinal e a discussão de estratégias que promovam proteção cruzada perante diversidade genotípica.
No contexto português, a distribuição genotípica descrita é consistente com tendências internacionais: PCV2d mantém-se como o genótipo mais frequentemente identificado, embora PCV2a permaneça com prevalência relevante, e podem ocorrer explorações com co-circulação de mais do que um genótipo. Considerando que múltiplos genótipos podem coexistir no terreno e variar ao longo do tempo, a avaliação por EpiCC constitui uma ferramenta adicional para explorar o possível impacto da divergência genética do vírus na cobertura de epítopos de células T pelas estirpes vacinais.
Paralelamente, a evolução do diagnóstico laboratorial tem acompanhado os avanços tecnológicos e o aumento do conhecimento científico, bem como a variabilidade genética dos microrganismos, permitindo disponibilizar ferramentas de diagnóstico de precisão, que apoiam a avaliação da diversidade genética de vírus (como por exemplo teste PCR Multiplex para tipificação de PCV2 nos subtipos PCV2a, PCV2b e PCV2d.) e bactérias presentes nas explorações. Uma publicação recente da Vetdiagnos demonstrou que a análise de amostras provenientes de 12 explorações de suiniculturas portuguesas permitiu observar que o subtipo PCV2d foi o mais frequente e que ocorreu a presença de mais do que um subtipo em 21% das amostras analisadas, reforçando a complexidade da infeção em condições de campo e a possibilidade de coexistência de múltiplas estirpes/genótipos. (dados Vetdiagnos publicados em 3 de Março de 2026 in LinkedIn)
Em particular, estes resultados suportam a hipótese de que combinações de estirpes vacinais (p.ex., PCV2a e PCV2b) possam contribuir para uma cobertura mais ampla de estirpes atuais e emergentes, devendo, contudo, esta interpretação ser enquadrada nas limitações inerentes a métricas preditivas e validada com evidência clínica e epidemiológica.
A Zoetis, através dos seus serviços técnicos, pode apoiar a identificação das estirpes de PCV2 circulantes na exploração; com base nessa caracterização, o CircoMatch™ pode ser utilizado para comparar a correspondência, ao nível de epítopos de células T (abordagem EpiCC/PigMatrix), entre estirpes de campo e vacinas disponíveis, fornecendo uma estimativa preditiva de cobertura que auxilia a seleção da opção vacinal.
Por fim, é plausível que uma monitorização regular do genótipo de PCV2 na mesma exploração evidencie variação temporal, potencialmente influenciada por fatores como a dinâmica de introdução/recirculação viral e pressões seletivas associadas à imunidade induzida por vacinação.
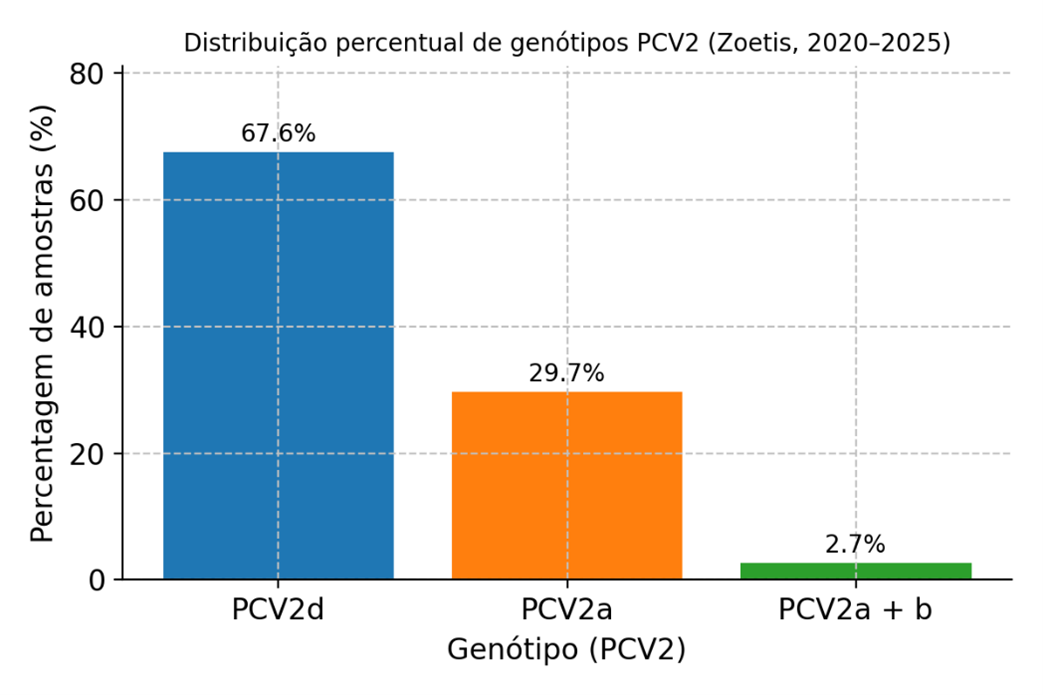
Gráfico 1 - Pesquisas internas Zoetis desde 2020
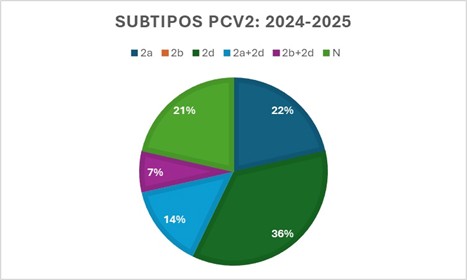
Gráfico 2 – Resultados Vetdiagnos de 12 explorações pelo teste de PCR Multiplex de Tipificação de P
CV2
Referencias:
- Franzo G, Segalés J. PLOS ONE. 2018. doi:10.1371/journal.pone.0208585.
- Karuppannan AK, Opriessnig T. Viruses. 2017. doi:10.3390/v9050099.
- Franzo G, Segalés J. Pathogens. 2020. doi:10.3390/pathogens9121049.
- Franzo G, Tucciarone CM, Legnardi M, Drigo M, Segalés J. Frontiers in Microbiology. 2024. doi:10.3389/fmicb.2024.1500498.
- Bandrick M, Gutiérrez AH, Desai P, Rincon G, Martin WD, Terry FE, De Groot AS, Foss DL. T cell epitope content comparison (EpiCC) analysis demonstrates a bivalent PCV2 vaccine has greater T cell epitope overlap with field strains than monovalent PCV2 vaccines. Internet. PubMed cited 2026 Feb 25. Available from: https://pubmed.ncbi.nlm.nih.gov/32278900/.
- Link EK, Eddicks M, Nan L, Ritzmann M, Sutter G, Fux R. Discriminating the eight genotypes of the porcine circovirus type 2 with TaqMan-based real-time PCR. Virol J. 2021;18:70. doi:10.1186/s12985-021-01541-z. link.springer
- Eddicks M, Ladurner Avilés S, Frauscher S, Krejici R, Reese S, Fux R, Ritzmann M. Update on the Prevalence of the PCV2 Major Genotypes PCV2a, PCV2b, and PCV2d in German Fattening Farms in 2024. Vet Sci. 2025;12(8):717. doi:10.3390/vetsci12080717. Mdpi
- Vetdiagnos in LinkedIn 3 de Março de 2026

